Προεμφυτευτική γενετική διάγνωση….ασφαλής λύση σε επιλεγμένες περιπτώσεις!!
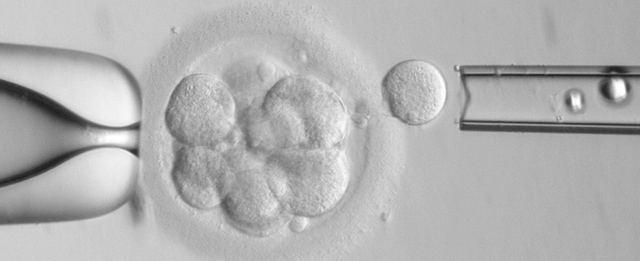
Η ΦΩΤΟΓΡΑΦΙΑ ΤΑ ΛΕΕΙ ΟΛΑ…Η ΠΑΡΕΜΒΑΣΗ ΓΙΝΕΤΑΙ Σ ΑΥΤΟ ΑΚΡΙΒΩΣ ΤΟ ΣΤΑΔΙΟ!
H Προεμφυτευτική Γενετική Διάγνωση (ΠΓΔ) προσφέρει τη δυνατότητα γενετικής διάγνωσης και μεταφοράς στη μήτρα μόνο των υγιών από τα έμβρυα που προέκυψαν από εξωσωματική γονιμοποίηση (in vitro fertilization “IVF”). H όλη διαδικασία είναι σήμερα εφικτή λόγω της εξέλιξης τριών διαφορετικών τομέων της βιοτεχνολογίας: την εξωσωματική γονιμοποίηση, την εμβρυολογία και τη γενετική διάγνωση. Η πρώτη εφαρμογή ΠΓΔ στην κλινική πράξη έγινε το 1990 από την ομάδα του Handyside, στο νοσοκομείο του Hammersmith στο Λονδίνο, για την επιλογή φύλου σε δύο ζευγάρια που αντιμετώπιζαν τον κίνδυνο να μεταβιβάσουν στους απογόνους τους φυλοσύνδετο νόσημα. Δύο χρόνια αργότερα η ίδια ομάδα για πρώτη φορά εφάρμοσε ΠΓΔ για υπολειπόμενη αυτοσωματική νόσο και συγκεκριμένα για Κυστική Ίνωση.
Προϋποθέσεις για την εφαρμογή ΠΓΔ είναι να αντιμετωπίζει το ζευγάρι τον κίνδυνο μεταβίβασης κάποιου γενετικού νοσήματος ή συγκεκριμένης χρωμοσωμικής διαταραχής στο έμβρυο και παράλληλα: α) να είναι υποχρεωμένο να καταφύγει σε μεθόδους υποβοηθούμενης αναπαραγωγής λόγω υπογονιμότητας ή β) να έχει ιστορικό πολλαπλών διακοπών κυήσεων μετά από προγεννητική διάγνωση με παθολογικό αποτέλεσμα ή γ) να πάσχει η σύζυγος από κάποιο χρόνιο νόσημα με κίνδυνο επιβάρυνσης της γενικής της κατάστασης από διακοπή μιας κύησης (π.χ. μεσογειακή αναιμία), ή δ) να προβάλλονται ηθικοί-θρησκευτικοί ενδοιασμοί για διακοπή κύησης, όταν κατά τον προγεννητικό έλεγχο αποκαλύπτεται παθολογικό έμβρυο.Η ΠΓΔ εφαρμόζεται σήμερα τόσο για την αποφυγή χρωμοσωμικών ανωμαλιών (ανευπλοειδίες, χρωμοσωμικές μεταθέσεις, ελλείμματα, αναστροφές) όσο και μονογονιδιακών νοσημάτων (φυλοσύνδετα, αυτοσωματικά υπολειπόμενα, αυτοσωματικά επικρατητικά, μιτοχονδριακά).
Υποβοηθούμενη αναπαραγωγή και πηγές εμβρυϊκού γενετικού υλικού στην ΠΓΔ
Tο στάδιο της εξωσωματικής γονιμοποίησης καθώς και η εμβρυομεταφορά γίνονται σε εξειδικευμένο κέντρο υποβοηθούμενης αναπαραγωγής. Για την εφαρμογή ΠΓΔ απαιτούνται όλα τα στάδια της εξωσωματικής γονιμοποίησης που περιλαμβάνουν: διέγερση των ωοθηκών, γονιμοποίηση των ωαρίων με ενδοκυτταρική έγχυση σπερματοζωαρίου (Intra Cytoplasmic Sperm Injection-ICSI) διαδικασία απαραίτητη στις περιπτώσεις ΠΓΔ μονογονιδιακών νοσημάτων και καλλιέργεια των εμβρύων. Πριν το επόμενο στάδιο που είναι η εμβρυομεταφορά διενεργείται βιοψία των εμβρύων ώστε να εξασφαλιστεί γενετικό υλικό στο οποίο θα γίνει η γενετική διάγνωση.
Υπάρχουν τρία είδη κυττάρων τα οποία μπορούν να επιλεγούν για γενετική διάγνωση στην ΠΓΔ: πολικό σωμάτιο, βλαστομερίδιο ή κύτταρα από την εξωτερική στοιβάδα βλαστοκύστης. Σε κάθε περίπτωση απαιτείται διάνοιξη της διαφανούς ζώνης (zona pellucida) που επιτυγχάνεται συνήθως είτε με χημική επεξεργασία (με Acid Tyrode’s) είτε με χρησιμοποίηση Laser. Η κάθε μια από τις τρεις επιλογές κυττάρων που αναφέρθηκαν, έχει πλεονεκτήματα και μειονεκτήματα.
Α) Βιοψία των πολικών σωματίων (polar body biopsy).
Η βιοψία του πρώτου και δευτέρου
πολικού σωματίου γίνεται την ημέρα της
ωοληψίας. Τα πολικά σωμάτια δημιουργούνται
αμέσως μετά τη γονιμοποίηση, μετά την
πρώτη και δεύτερη μειωτική διαίρεση
του ωαρίου και η γενετική διάγνωση
αποσκοπεί στην επιλογή υγιών ωαρίων.
Στις περιπτώσεις που
η υποψήφια μητέρα φέρει αυτοσωματικό
επικρατητικό νόσημα, η βιοψία των πολικών
σωματίων επιτρέπει την επιλογή των
φυσιολογικών ωαρίων για γονιμοποίηση,
εξασφαλίζοντας φυσιολογικά έμβρυα.
Στην περίπτωση όμως των φυλοσύνδετων
ή αυτοσωματικών υπολειπόμενων νοσημάτων,
η απόρριψη ενός παθολογικού ωαρίου που
φέρει τη μετάλλαξη στερεί τη δυνατότητα
να γονιμοποιηθεί με ένα φυσιολογικό
πατρικό γαμετικό κύτταρο και να
δημιουργηθεί ένας φυσιολογικός
οργανισμός.
Η βιοψία πολικού σωματίου
είναι προτιμότερη αφού γίνεται σε
κύτταρα που απορρίπτονται κατά την
ανάπτυξη του εμβρύου. Για το λόγο αυτό
αποτελεί τη μοναδική ηθικά αποδεκτή
λύση για την εφαρμογή ΠΓΔ στα κράτη
εκείνα όπου ο έλεγχος στα έμβρυα δεν
είναι επιτρεπτός, όπως για παράδειγμα,
στη Γερμανία και στην Ιταλία. Μειονεκτεί
όμως διότι η διαδικασία απομόνωσης των
πολικών σωματίων είναι δύσκολη, η
γενετική διάγνωση των ωαρίων είναι
έμμεση, ο γονότυπος του πατρικού γαμετικού
κυττάρου παραμένει άγνωστος, ενώ
οποιεσδήποτε ανωμαλίες που μπορεί να
προκύψουν μετά τη γονιμοποίηση, δεν
είναι δυνατό να εντοπιστούν.
Β) Bιοψία βλαστομεριδίων
(cleavage stage embryo biopsy)
H βιοψία βλαστομεριδίων
γίνεται την τρίτη μέρα μετά τη γονιμοποίηση,
όταν το έμβρυο βρίσκεται στη φάση των
6-8 κυττάρων. Το βλαστομερίδιο είναι μη
διαφοροποιημένο εμβρυϊκό κύτταρο που
απομονώνεται σχετικά εύκολα καθώς σε
αυτό το στάδιο ανάπτυξης τα κύτταρα δεν
έχουν αναπτύξει ακόμα τους ισχυρούς
δεσμούς που δημιουργούνται στο μορίδιο.
Με τη μέθοδο αυτή υπάρχει αρκετός χρόνος
για να ολοκληρωθεί η διάγνωση μέχρι την
εμβρυομεταφορά, που πραγματοποιείται
την τέταρτη ή πέμπτη ημέρα και σπανιότερα
την έκτη μέρα της ανάπτυξης του εμβρύου.
Τα βλαστομερίδια
αποτελούν την προτιμώμενη πηγή εμβρυικού
γενετικού υλικού από τα περισσότερα
κέντρα που προσφέρουν ΠΓΔ. Παρ όλα αυτά
υπάρχει προβληματισμός για τον προτιμώμενο
αριθμό των βλαστομεριδίων (ένα ή δύο)
που πρέπει να ληφθούν. Πολλοί ερευνητές
έχουν μελετήσει τις πιθανές επιπτώσεις
της αφαίρεσης ενός, σε σύγκριση με την
αφαίρεση περισσότερων κυττάρων κατά
τη διάρκεια της βιοψίας, αξιολογώντας
την περαιτέρω ανάπτυξη του εμβρύου, την
πιθανότητα εμφύτευσης, το ποσοστό των
εμβρύων που διαγιγνώσκονται καθώς και
την πιθανότητα σφάλματος στη διάγνωση.
Στην πράξη, καθώς δεν υπάρχει επίσημη
επιστημονική θέση, το κάθε κέντρο
υποβοηθούμενης αναπαραγωγής λειτουργεί
με βάση τη δική του εκτίμηση στο θέμα
αυτό.
Γ) Βιοψία κυττάρων από
βλαστοκύστη (blastocyst stage biopsy)
Η βιοψία
κυττάρων από βλαστοκύστη γίνεται την
πέμπτη ή έκτη ημέρα μετά τη γονιμοποίηση
και αφορά τη λήψη κυττάρων από την
εξωτερική κυτταρική μάζα της βλαστοκύστης,
η οποία στη συνέχεια θα εξελιχθεί στις
χορειακές λάχνες του εμβρύου (trophectoderm
layer). Πρόκειται για μια διαδικασία που
θα μπορούσε να θεωρηθεί ως πολύ πρώιμη
λήψη τροφοβλάστης. Προσφέρει το
πλεονέκτημα ότι επιτρέπει τη βιοψία
περισσότερων κυττάρων για γενετική
ανάλυση (10-20 κύτταρα), διευκολύνοντας
τη διάγνωση. Η λήψη περισσότερων κυττάρων
εξασφαλίζει αντιπροσωπευτικότερη
εικόνα του εμβρύου στα κύτταρα που
αναλύονται περιορίζοντας τον κίνδυνο
σφάλματος λόγω μωσαϊκισμού (συναντάται
σε συχνότητα ~50% στα έμβρυα στο
προεμφυτευτικό στάδιο της ανάπτυξης).
Επί πλέον οι βλαστοκύστεις που έχουν
υποστεί βιοψία έχουν μεγαλύτερες
πιθανότητες εμφύτευσης σε σχέση με τα
έμβρυα τρίτης ημέρας. Παρ όλα αυτά
υπάρχουν και μειονεκτήματα όπως: η
δυσκολία της βιοψίας σε αυτό το στάδιο
της ανάπτυξης του εμβρύου, ο μικρότερος
αριθμός των διαθέσιμων εμβρύων (λιγότερα
από το 50% φτάνουν σε αυτό το στάδιο
ανάπτυξης) και ο περιορισμένος διαθέσιμος
χρόνος για τη γενετική διάγνωση. Τελευταία
επίσης μεγάλος προβληματισμός υπάρχει
για την παράταση της καλλιέργειας των
εμβρύων και την επίπτωση των καλλιεργητικών
μέσων στην αύξηση της συχνότητας των
νοσημάτων που οφείλονται στη γονιδιακή
αποτύπωση (imprinting).
Γενετική ανάλυση στην
ΠΓΔ
H γενετική ανάλυση πρέπει να
εξασφαλίσει αξιόπιστη διάγνωση σε
ελάχιστη ποσότητα DNA και σε περιορισμένο
χρονικό διάστημα (έως και ένα
εικοσιτετράωρο), ώστε η εμβρυομεταφορά
να γίνει έγκαιρα, χωρίς να υπάρχουν
επιπτώσεις στην ποιότητα και βιωσιμότητα
του εμβρύου από παρατεταμένη εξωμήτρια
παραμονή. Διαφορετικές μεθοδολογίες
χρησιμοποιούνται στην ΠΓΔ για χρωμοσωμικές
ανωμαλίες σε σχέση με αυτές για τα
μονογονιδιακά νοσήματα.
1. Εφαρμογή ΠΓΔ για
Χρωμοσωμικές Ανωμαλίες
Η βασική
μέθοδος που εφαρμόζεται για ΠΓΔ
χρωμοσωμικών ανωμαλιών από τα περισσότερα
κέντρα παγκοσμίως είναι ο φθορίζων «in
situ» υβριδισμός (Fluorecsence In Situ Hybridization,
FISH). Πρόκειται για στοχευμένο έλεγχο
συγκεκριμένων χρωμοσωμάτων σε μεσοφασικούς
πυρήνες εμβρυϊκών κυττάρων. Τα κύτταρα
μονιμοποιούνται σε αντικειμενοφόρες
πλάκες και τα χρωμοσώματα ανιχνεύονται
με υβριδοποίηση με ανιχνευτές σημασμένους
με φθορίζουσες χρωστικές, οι οποίοι
είναι συμπληρωματικοί με περιοχές των
χρωμοσωμάτων που ελέγχονται κάθε φορά.
Η μέθοδος αρχικά εφαρμόστηκε κυρίως για την αποφυγή χρωμοσωμικών ανωμαλιών που υπάρχουν στην οικογένεια, όπως αμοιβαίες μεταθέσεις (reciprocal translocations), ή μεταθέσεις ακροκεντρικών χρωμοσωμάτων 13, 14, 15, 21 και 22 (Robertsonian translocations).
Τα πρωτόκολλα που εφαρμόζονται για ΠΓΔ με FISH για την αποφυγή γενετικών διαταραχών που οφείλονται στην ύπαρξη αμοιβαίων χρωμοσωμικών μεταθέσεων εξατομικεύονται για κάθε περιστατικό. Αναλυτικότερα, σχεδιάζονται χρωμοσωμικοί ανιχνευτές συμπληρωματικοί των περιοχών των χρωμοσωμάτων, που προβλέπεται (από την μετάθεση που φέρει ο υποψήφιος γονέας) να εμφανίσουν διπλασιασμό ή έλλειμμα στα έμβρυα, ώστε να επιλέγονται έμβρυα με ισοζυγισμένο γενετικό υλικό. Στην περίπτωση μεταθέσεων ακροκεντρικών χρωμοσωμάτων η διαδικασία είναι απλούστερη, αφού για την κλινική εφαρμογή της ΠΓΔ δεν απαιτείται παρά η χρήση των κοινών ανιχνευτών που χρησιμοποιούνται για τα συγκεκριμένα χρωμοσώματα.
Άλλη εφαρμογή της μεθόδου FISH σε συνδυασμό με ΠΓΔ είναι για την εντόπιση αριθμητικών χρωμοσωμικών ανωμαλιών (ανευπλοειδίες). Η υψηλή συχνότητα ανευπλοειδιών σε ανθρώπινα ωάρια, κυρίως γυναικών μεγαλύτερων των 40 ετών, καθώς και σε έμβρυα που βρίσκονται στα πρώτα στάδια της ανάπτυξης (μεγαλύτερο του 50% και του 60% αντίστοιχα) είναι ένα γεγονός που έχει διαπιστωθεί εδώ και πολλά χρόνια. Αυτός είναι και ο λόγος που πολύ νωρίς, άρχισε να εφαρμόζεται από πολλά κέντρα παγκοσμίως μια τακτική ελέγχου χρωμοσωμάτων, γνωστή ως Preimplantation Genetic Screening (PGS). Η τακτική αυτή στοχεύει στον αποκλεισμό για εμβρυομεταφορά των ανευπλοειδικών εμβρύων και κατά συνέπεια στην αύξηση της επιτυχίας της εξωσωματικής γονιμοποίησης. Ο περιορισμός της μεθόδου FISH αφορά στον αριθμό των ανιχνευτών που μπορεί να χρησιμοποιηθούν ταυτόχρονα σε ένα κύτταρο, που δεν μπορεί να ξεπεράσει τους πέντε, ενώ η επανυβριδοποίηση με άλλους μειώνει τη διακριτική ικανότητα της τεχνικής, περιορίζοντας έτσι τον αριθμό των χρωμοσωμάτων που μπορούν να ελεγχθούν ανά κύτταρο (δεν ξεπερνούν τους 15). Κατά συνέπεια για την PGS επελέγη να γίνεται έλεγχος εκείνων των ανευπλοειδιών που συναντώνται συχνότερα στις αυτόματες αποβολές και σε παθολογικά έμβρυα και που αφορούν συγκεκριμένα τα χρωμοσώματα Χ, Υ, 13, 16, 18, 21, και 22.
Η PGS προτείνεται και προσφέρεται σε ζευγάρια με φυσιολογικό καρυότυπο που έχουν : α) πολλές παλίνδρομες κυήσεις ή β) περισσότερες από τρεις αποτυχημένες προσπάθειες IVF ή γ) προχωρημένη ηλικία της υποψήφιας μητέρας και δ) στις περιπτώσεις IVF που χρησιμοποιείται βιοψία όρχεος. Από συγκριτικές μελέτες όμως δεν διαπιστώνεται διαφορά στην επιτυχία της IVF όταν συνδυάζεται με PGS για τα παραπάνω χρωμοσώματα με FISH. Τα αποτελέσματα των μελετών αυτών τροφοδότησαν ένα πλήθος από συζητήσεις και προβληματισμούς στο χώρο της υποβοηθούμενης αναπαραγωγής ως προς τη χρησιμότητα του PGS με FISH και την εφαρμογή του σαν μέθοδο ρουτίνας στην IVF.
Η ανάπτυξη της τεχνικής του γενομικού συγκριτικού υβριδισμού (Comparative Genomic Hybridization, CGH) έδωσε πολλές νέες πληροφορίες για τη συχνότητα και το είδος των ανευπλοειδιών σε γαμετικά και εμβρυϊκά κύτταρα. Η τεχνική αυτή βασίζεται στον ανταγωνιστικό υβριδισμό μεταξύ ενός κατακερματισμένου δείγματος DNA και σημασμένου με φθορίζουσα χρωστική (πράσινη), με το DNA ενός φυσιολογικού μάρτυρα σημασμένου με μια άλλη φθορίζουσα χρωστική (κόκκινη) πάνω στα φυσιολογικά χρωμοσώματα ενός μεταφασικού πυρήνα που έχει μονιμοποιηθεί σε αντικειμενοφόρο πλάκα. Ο λόγος μεταξύ των δυο χρωστικών κατά μήκος των χρωμοσωμάτων ελέγχεται μέσω μικροσκοπίου και καταγράφεται με κατάλληλο λογισμικό. Ο λόγος της έντασης των δυο χρωστικών σε κάθε σημείο του χρωμοσώματος είναι ενδεικτικός για έλλειμμα ή πλεόνασμα χρωμοσωμικού υλικού στη θέση αυτή.
Αναλυτικότερα η τεχνική CGH έδωσε τη δυνατότητα ελέγχου όλων των χρωμοσωμάτων ταυτόχρονα και αποκάλυψε ότι το 20-30% των ωαρίων είναι ανευπλοειδικά σε ηλικίες από 20-30 ετών, ενώ για γυναίκες μεγαλύτερες των 40 ετών τα ποσοστά ανευπλοειδικών ωαρίων κυμαίνονται από 50-80%. Μόνο το 25% των εμβρύων στο στάδιο της αυλάκωσης αποτελούνται αμιγώς από ευπλοειδικά κύτταρα. Από τα ανευπλοειδικά έμβρυα, περίπου το 50% έχουν τις ίδιες ανευπλοειδίες σε όλα τα κύτταρα τους (δημιουργήθηκαν κατά τη μείωση) ενώ τα υπόλοιπα έμβρυα είναι «χαοτικά», δηλαδή έχουν διαφορετικές ανευπλοειδίες σε κάθε κύτταρό τους (δημιουργήθηκαν κατά τις μιτωτικές διαιρέσεις του εμβρύου). Από μελέτες φαίνεται επίσης ότι στα γαμετικά κύτταρα και στα έμβρυα παρατηρούνται ανευπλοειδίες σε όλα τα χρωμοσώματα, σε διαφορετική συχνότητα το κάθε ένα και ότι οι συχνότερες από αυτές, είναι διαφορετικές από εκείνες που συναντώνται στα κυοφορούμενα έμβρυα ή σε έμβρυα από αυτόματες αποβολές. Με την τεχνική CGH εκτιμήθηκε ότι μόνο το 20-40% των εμβρύων που φέρουν χρωμοσωμικές ανωμαλίες ανιχνεύονται με FISH, όταν στoχεύονται τα χρωμοσώματα Χ, Υ, 13, 16, 18, 21 και 22. Αν όμως επιλεγούν στην FISH όχι αυτά, αλλά εκείνα τα 10 χρωμοσώματα που εμφανίζουν συχνότερα ανευπλοειδίες σε γαμετικά κύτταρα και έμβρυα, τότε περισσότερα από το 85% των ανευπλοειδικών εμβρύων θα εντοπίζονται. Συμπερασματικά, η εφαρμογή PGS με CGH αυξάνει την πιθανότητα εγκυμοσύνης και εμφύτευσης ενός επιλεγμένου εμβρύου. Το βασικό μειονέκτημα της μεθόδου του CGH κατά την κλινική εφαρμογή PGS είναι η δυσκολία στη διάγνωση, για την οποία απαιτείται μεγάλη εμπειρία στην κυτταρογενετική. Επίσης απαιτείται και ο αυξημένος χρόνος για την ολοκλήρωση της γενετικής διάγνωσης (περίπου 4 εικοσιτετράωρα). Αυτό επιβάλλει την κατάψυξη των εμβρύων και μεταφορά των ευπλοειδικών σε επόμενο κύκλο, με επίπτωση φυσικά στη βιωσιμότητα τους, λόγω της αναγκαίας απόψυξης.
Ένα νέο μεγάλο κεφάλαιο έχει δημιουργηθεί πρόσφατα στο χώρο της PGS, με την ανάπτυξη πολύ ευαίσθητων τεχνικών και την εφαρμογή νέων τεχνολογιών που επιτρέπουν κυτταρογενετικό έλεγχο υψηλής ανάλυσης. Βασίζονται στη χρησιμοποίηση των μικροσυστοιχιών και επιτρέπουν τον έλεγχο ολόκληρου του γονιδιώματος. Μελέτες έχουν δείξει πως οι τεχνικές αυτές μπορούν να προσαρμοστούν κατάλληλα ώστε να εφαρμοστούν στο επίπεδο του ενός κυττάρου:
α) Γενομικός συγκριτικός υβριδισμός σε μικροσυστοιχίες ολιγονουκλεοτιδίων (array-CGH).Το σημασμένο με φθορίζουσα χρωστική DNA υβριδοποιείται πάνω σε ολιγονουκλεοτίδια ακινητοποιημένα πάνω σε ειδική αντικειμενοφόρο πλάκα και όχι πάνω σε μεταφασικά χρωμοσώματα, όπως στην CGH. Τo κάθε ολιγονουκλεοτίδιο έχει καθορισμένη θέση πάνω στην πλάκα και είναι συμπληρωματικό για μια συγκεκριμένη περιοχή στο γονιδίωμα. Η μέθοδος έχει όλα τα πλεονεκτήματα του CGH, όμως είναι πιο γρήγορη (2 εικοσιτετράωρα) και επιτρέπει εμβρυομεταφορά στον ίδιο κύκλο IVF. Δοκιμές έχουν γίνει για την ελάττωση του χρόνου διάγνωσης σε 10 ώρες.
Η πρώτη κλινική εφαρμογή PGS με array-CGH που έγινε χρησιμοποιώντας ολιγονουκλεοτίδια ανιχνευτές έχει οδηγήσει σε εγκυμοσύνες χωρίς την ανάγκη της κατάψυξης εμβρύων. Για να είναι όμως αξιόπιστη η ανάλυση θα πρέπει να χρησιμοποιείται μεγάλος αριθμός ολιγονουκλεοτιδίων ανιχνευτών, γεγονός που αυξάνει το κόστος ανά κύτταρο που εξετάζεται.
β) Γενομικός
συγκριτικός υβριδισμός σε μικροσυστοιχίες
βακτηριδιακών συνθετικών χρωμοσωμάτων
BAC-arrays (Bacterial Artificial Chromosomes). Στην
περίπτωση αυτή στην αντικειμενοφόρο
πλάκα ακινητοποιούνται χιλιάδες τμήματα
DNA. Το καθ’ ένα είναι συμπληρωματικό με
μια περιοχή ενός χρωμοσώματος που έχει
μέγεθος από 150 έως 200kb (BAC clones). Το βασικό
πρόβλημα στην εφαρμογή της τεχνικής
αυτής είναι η έλλειψη επαναληψιμότητας
που οφείλεται στην κατασκευή των πλακών.
Παρ όλα αυτά τα τελευταία χρόνια ένα
πλήθος από μεμονωμένα κύτταρα, πολικά
σωμάτια και βλαστομερίδια έχουν ελεγχθεί
με επιτυχία με την τεχνική αυτή.
γ) Γενομικός
συγκριτικός υβριδισμός σε μικροσυστοιχίες
βιβλιοθηκών DNA συμπληρωματικών στα
χρωμοσώματα (Chromosome libraries). Η πολλά
υποσχόμενη αυτή τεχνική φαίνεται να
έχει μικρότερο κόστος. Το μειονέκτημά
της είναι η δυσκολία να εντοπίσει
ελλείμματα ή διπλασιασμούς σε μικρές
χρωμοσωμικές περιοχές. Επομένως, αν και
είναι κατάλληλη για PGS, δεν μπορεί να
εφαρμοστεί για ΠΓΔ αμοιβαίων μεταθέσεων
(reciprocal translocations).
δ) Μικροσυστοιχίες
που ανιχνεύουν σημειακές αλλαγές κατά
μήκος του γονιδιώματος (SNP-microarrays). H
τεχνική αυτή μπορεί να ανιχνεύσει από
10.000 έως 500.000 σημειακές αλλαγές κατά
μήκος ολόκληρου του γονιδιώματος και
έχει μια εντελώς διαφορετική λογική σε
σχέση με τις παραπάνω προσεγγίσεις του
συγκριτικού υβριδισμού. Το κατακερματισμένο
DNA του υπό εξέταση δείγματος υβριδοποιείται
σε διαφορετική θέση από το DNA αναφοράς
πάνω στην ίδια αντικειμενοφόρο πλάκα,
ενώ και τα δύο σημαίνονται με την ίδια
φθορίζουσα ομάδα. O αριθμός των αντιγράφων
του χρωμοσώματος μπορεί να προσδιοριστεί
παράλληλα με δυο τρόπους: α) Ανάλυση
σύνδεσης (linkage analysis). Παραβάλλοντας τα
εμβρυϊκά αλληλόμορφα SNPs με αυτά των δυο
γονέων εντοπίζει τη γονεϊκή προέλευση
του κάθε χρωμοσώματος. Η κληρονόμηση
τριών διαφορετικών απλοτύπων δηλώνει
τρισωμία, ενώ η ομοζυγωτία όλων των SNPs
κατά μήκος ενός χρωμοσώματος δηλώνει
μονοσωμία. β) Σύγκριση της έντασης του
φθορισμού στα SNPs που αντιστοιχούν σε
κάποιο χρωμόσωμα, μεταξύ του υπό εξέταση
δείγματος και του δείγματος αναφοράς.
Εντοπίζει ανευπλοειδία (περίσσεια ή
έλλειψη χρωμοσώματος) αλλά και μικρότερα
ελλείματα/διπλασιασμούς εξ αιτίας
μεταθέσεων (reciprocal and Robertsonian). Σε επίπεδο
ενός κυττάρου η τεχνική έχει εφαρμοστεί
με επιτυχία από τον Handyside και τους
συνεργάτες του το 2009.
Το βασικό μειονέκτημα όλων των προσεγγίσεων που αναφέρθηκαν προηγουμένως είναι το αυξημένο κόστος, λαμβάνοντας υπ’ όψη πως σε κάθε κύκλο είναι πολλά τα έμβρυα που θα πρέπει να ελεχθούν. Αν και τα δεδομένα από την εφαρμογή των τεχνικών αυτών είναι πολύ ενθαρρυντικά, απαιτούνται ακόμα πολλές δοκιμές και βελτιώσεις ώστε να εφαρμοστούν στην κλινική πράξη. Επίσης είναι σημαντικό να αξιολογηθεί ποιά προσέγγιση συνδυάζει μεγαλύτερη αξιοπιστία και ταχύτητα, με χαμηλότερο κόστος.
Πρέπει όμως να τονιστεί ότι αν και η ευρεία εφαρμογή της PGS στην κλινική πρακτική με την αξιοποίηση της νέας τεχνολογίας αποτελεί ελκυστικό στόχο, η PGS δεν πρόκειται να υπερπηδήσει ποτέ τον κίνδυνο της απόρριψης εμβρύων, τα οποία, αν και εμφανίζονται παθολογικά στο κύτταρο που αναλύεται, έχουν τη δυναμική να δώσουν υγιείς οργανισμούς μέσω του μηχανισμού της φυσικής διόρθωσης ανευπλοειδιών (chromosome rescue).
2. Εφαρμογή ΠΓΔ για
μονογονιδιακά νοσήματα
Σήμερα
ΠΓΔ μπορεί να εφαρμοστεί για όλα τα
μονογονιδιακά νοσήματα με γνωστή
γενετική διαταραχή, στα οποία
περιλαμβάνονται αυτοσωματικά υπολειπόμενα,
αυτοσωματικά επικρατητικά, φυλοσύνδετα
και μιτοχονδριακά (Πίνακας 1). Για τη
γενετική διάγνωση απαιτείται ο εξοπλισμός
και η τεχνογνωσία ενός εργαστηρίου
μοριακής γενετικής. Όλα τα πρωτόκολλα
ΠΓΔ μονογονιδιακών νοσημάτων βασίζονται
στην αλυσιδωτή αντίδραση της πολυμεράσης
(Polymerase Chain Reaction, PCR). Tα προβλήματα που
προκύπτουν γενικά κατά τη γενετική
διάγνωση με την εφαρμογή PCR, σε DNA που
προέρχεται από ένα και μόνο κύτταρο,
αφορούν την αποτυχία πολλαπλασιασμού
του DNA (amplification failure), το μη ισοδύναμο
πολλαπλασιασμό του DNA από τα δύο
αλληλόμορφα (allelic drop-out, ADO) και την
επιμόλυνση από ξένο DNA. Όλα αυτά μπορεί
να οδηγήσουν είτε σε αδυναμία διάγνωσης,
είτε σε λανθασμένη διάγνωση.
Για το σχεδιασμό ενός πρωτοκόλλου ΠΓΔ για μονογονιδιακό νόσημα θα πρέπει να λαμβάνεται υπ’ όψιν ο περιορισμένος αριθμός γενετικού υλικού που είναι διαθέσιμο για τη γενετική διάγνωση, η αδυναμία εφαρμογής περισσότερων της μιας αντίδρασης PCR καθώς και οι ιδιαιτερότητες του ίδιου του νοσήματος, όπως το μέγεθος του γονιδίου που ευθύνεται για το νόσημα, το πλήθος και η θέση των μεταλλάξεων στο γονίδιο.
Σε σχέση με την προηγούμενη δεκαετία, σήμερα ο εργαστηριακός (μοριακός βιολόγος-γενετιστής) έχει στη διάθεσή του βελτιωμένα ένζυμα πολυμερισμού του DNA, κατά την PCR, που εξασφαλίζουν πολύ καλύτερες αποδόσεις καθώς και πολύ ευαίσθητες τεχνικές, κυρίως φθορισμομετρικές, με χρήση νέων τεχνολογιών, για την ανίχνευση των προϊόντων της PCR.
Σήμερα συνιστάται, παράλληλα με το γονίδιο που ευθύνεται για το νόσημα που εξετάζεται, να γίνεται και έλεγχος πολυμορφικών μικροδορυφορικών αλληλουχιών ή σημειακών αλλαγών που βρίσκονται κοντά ή και μέσα στο γονίδιο αυτό, με σκοπό την έμμεση γενετική διάγνωση μέσω ανάλυσης σύνδεσης (linkage analysis). Με τον τρόπο αυτό επιτυγχάνεται μείωση της πιθανότητας λανθασμένης διάγνωσης, αντιμετωπίζεται το πρόβλημα του ADO, ελέγχεται η πιθανότητα επιμόλυνσης από ξένο DNA σε κάθε ένα έμβρυο ξεχωριστά, ενώ αυξάνεται ο αριθμός των εμβρύων που μπορούν να μεταφερθούν για εμφύτευση. Η παραπάνω διαδικασία είναι εφικτή με την εφαρμογή πολλαπλού PCR (multiplex PCR) που επιτρέπει τον πολλαπλασιασμό ταυτόχρονα πολλών τμημάτων DNA. Στην περίπτωση που το πρωτόκολλο απαιτεί τον πολλαπλασιασμό μεγάλου αριθμού τμημάτων DNA και η βελτιστοποίηση της PCR δημιουργεί δυσκολίες, υπάρχει και η δυνατότητα του ενζυμικού πολλαπλασιασμού ολόκληρου του γονιδιώματος του μεμονωμένου κυττάρου (whole genome amplification) με τεχνικές όπως primer extension preamplification (PEP) method, degenerate oligonucleotide primed PCR (DOP-PCR), tagged random primers PCR (T-PCR), linker- adaptor PCR (LAPCR), T7-based linear amplification of DNA (TLAD) και multiple displacement amplification (MDA). Με τον τρόπο αυτό εξασφαλίζεται μεγάλη ποσότητα DNA που αρκεί για πολλές διαφορετικές αντιδράσεις PCR. Όμως αν και η αύξηση της ποσότητας του γενετικού υλικού διευκολύνει πολύ το στάδιο της ανάπτυξης ενός πρωτοκόλλου ΠΓΔ, κατά την κλινική εφαρμογή παρατηρούνται πολύ αυξημένα επίπεδα ADO. Με το δεδομένο αυτό, για την εξασφάλιση αξιοπιστίας της διάγνωσης απαιτείται στη συνέχεια ο πολλαπλασιασμός και ανάλυση πολύ μεγάλου αριθμού μικροδορυφορικών αλληλουχιών που βρίσκονται σε σύνδεση με το υπεύθυνο γονίδιο, που όμως έχουν ως αποτέλεσμα την αύξηση του κόστους αλλά και του χρόνου της γενετικής διάγνωσης. Η δυνατότητα εφαρμογής της μεθόδου του πολλαπλού PCR ή και του πολλαπλασιασμού ολόκληρου του γονιδιώματος (επιτρέπει την έμμεση διάγνωση μέσω ανάλυσης σύνδεσης) διευκόλυνε την καθιέρωση πρωτοκόλλων ευρείας εφαρμογής για το κάθε νόσημα, περιορίζοντας την ανάγκη σχεδιασμού πρωτοκόλλων για κάθε ένα μεμονωμένο περιστατικό.
Τα τελευταία είκοσι χρόνια έχουν εφαρμοστεί πολλές τεχνικές για την ανίχνευση σημειακών αντικαταστάσεων, μικροελλειμμάτων ή μικροενθέσεων, όπως για παράδειγμα amplification refractory mutation system (ARMS), restriction fragment length polymorphism (RFLP), single stranded conformational polymorphism (SSCP) and heteroduplex analysis (HA) techniques. Στις νέες τεχνολογίες περιλαμβάνονται PCR πραγματικού χρόνου (Real Time PCR) ή αυτοματοποιημένα συστήματα ανάλυσης της πρωτοταγούς δομής του DNA (sequencing και mini-sequencing).
Όπως αναφέρθηκε και στο κεφάλαιο της εφαρμογής ΠΓΔ για χρωμοσωμικές ανωμαλίες, μια πολλά υποσχόμενη τεχνική στο χώρο της ΠΓΔ είναι τα SNP-microarrays. Αν και η μέθοδος δεν έχει εφαρμοστεί ακόμα κλινικά, με βάση τις δοκιμές που έχουν γίνει σε μεμονωμένα λεμφοκύτταρα από τον Handyside και τους συνεργάτες του το 2009, οι οποίοι χρησιμοποίησαν ως μοντέλο μονογονιδιακού νοσήματος την Κυστική Ίνωση, φαίνεται ότι θα μπορούσε να χρησιμοποιηθεί για οποιοδήποτε μονογονιδιακό νόσημα, ενώ παράλληλα επιτρέπει τον έλεγχο ανευπλοειδιών ή άλλων χρωμοσωμικών διαταραχών που πιθανό συνυπάρχουν. Η εξέλιξη της τεχνολογίας, σε συνδυασμό με την άμεση πρόσβαση σε ηλεκτρονικές βάσεις γενετικών δεδομένων και λογισμικών, επιτρέπουν σε ένα σύγχρονο εργαστήριο γενετικής τη δυνατότητα σχεδιασμού και κλινικής εφαρμογής ΠΓΔ για οποιοδήποτε μονογονιδιακό νόσημα, έστω και αν αυτό είναι σπάνιο. H στρατηγική ανάπτυξης πρωτοκόλλων ΠΓΔ περιλαμβάνει τα εξής στάδια:
•Εύρεση της μετάλλαξης
ή των μεταλλάξεων που ευθύνονται για
το νόσημα και εντοπισμός πολυμορφικών
μικροδορυφορικών αλληλουχιών που
βρίσκονται σε σύνδεση (linked) με το υπεύθυνο
για το νόσημα γονίδιο, μέσω ηλεκτρονικών
βάσεων δεδομένων όπως ENSEMBL, UCSC,
uniSTS.
•Ανάλυση σύνδεσης (linkage analysis) των
πολυμορφικών αλληλουχιών με το υπεύθυνο
γονίδιο στην οικογένεια για τον εντοπισμό
των πληροφοριακών αλληλομόρφων.
•Σχεδιασμός
της multiplex PCR μέσω λογισμικών όπως IDT,
In-Silico PCR
•Βελτιστοποίηση της μεθόδου
σε αραιωμένο γενομικό DNA από τα μέλη της
οικογένειας•Εκτίμηση της αξιοπιστίας
και της ευαισθησίας της μεθόδου σε DNA
από μεμονωμένα λεμφοκύτταρα των υποψήφιων
γονέων (σύμφωνα με τις προδιαγραφές του
PGD Consortium της ESHRE)
•Εφαρμογή της μεθόδου
σε μεμονωμένα βλαστομερίδια από προς
απόρριψη έμβρυα που έχουν γονιμοποιηθεί
εξωσωματικά.
•Κλινική εφαρμογή
Για να χρησιμοποιηθεί ένα πρωτόκολλο ΠΓΔ στην κλινική πράξη θα πρέπει να έχει εξασφαλιστεί ικανοποιητικός πολλαπλασιασμός της περιοχής ή των περιοχών του γονιδίου όπου εντοπίζονται οι μεταλλάξεις που ευθύνονται για το νόσημα. Επίσης θα πρέπει να έχει επιλεγεί και προτυποποιηθεί η κατάλληλη κάθε φορά μέθοδος ανίχνευσης των μεταλλάξεων, ώστε να εξασφαλίζεται η αξιοπιστία της γενετικής διάγνωσης. Σύμφωνα με τις προδιαγραφές, όπως έχουν καθοριστεί από το European Society of Human Reproduction and Embryology (ESHRE), για να εφαρμοστεί σε κλινικό επίπεδο μια μέθοδος ΠΓΔ θα πρέπει να έχει περιοριστεί η ολοκληρωτική αποτυχία του πολλαπλασιασμού σε επίπεδα μικρότερα του 10% και του ADO σε μικρότερα του 5%. Ο έλεγχος για την αξιολόγηση ενός πρωτοκόλλου οφείλει να είναι αυστηρός και το πρωτόκολλο να διαθέτει δικλείδες ασφαλείας ώστε να εντοπίζεται και να αξιολογείται τόσο το ADO όσο και η επιμόλυνση. Η ΠΓΔ επιβάλλεται να εφαρμόζεται από έμπειρους επιστήμονες σε κατάλληλους χώρους που πληρούν τις προδιαγραφές για την ελαχιστοποίηση της πιθανότητας επιμόλυνσης. Τέλος η επιτυχία της προσπάθειας προϋποθέτει και την καλή ποιότητα του κυττάρου (του υλικού) που αποστέλλεται για διάγνωση από τον εμβρυολόγο. Η ολοκληρωτική όσο και η μερική αποτυχία πολλαπλασιασμού του DNA (ADO), μπορεί να οφείλεται είτε στην απώλεια του κυττάρου κατά τη μεταφορά του στο σωληνάριο που γίνεται η αντίδραση PCR, είτε στη βιοψία ενός απύρηνου ή κακής ποιότητας κυττάρου ή ακόμα στην ατελή λύση της κυτταρικής μεμβράνης.
Η εμπειρία του
Εργαστηρίου Ιατρικής Γενετικής στην
ΠΓΔ μονογονιδιακών νοσημάτων
Τα
τελευταία 13 χρόνια στο εργαστήριο
Ιατρικής Γενετικής του Πανεπιστημίου
Αθηνών αναπτύξαμε και εφαρμόσαμε ΠΓΔ
για ένα πλήθος μονογονιδιακών νοσημάτων,
όπως: τα μεσογειακά σύνδρομα, η κυστική
ίνωση (ΚΙ), η νωτιαία μυϊκή ατροφία (SMA),
φυλοσύνδετα ή φυλοεξαρτώμενα γονίδια
όπως η μυϊκή δυστροφία Duchenne, το σύνδρομο
του εύθραυστου Χ και η λιποειδής
υπερπλασία των επινεφριδίων (Congenital
Lipoid Adrenal Hyperplasia – CLAH). Επίσης ασχοληθήκαμε
και με σπάνια νοσήματα όπως η γλυκογονίαση
(Glycogen Storage Disease - GSD), η συγγενής αμαύρωση
Leber (Leber’s Congenital Amaurosis - LCA), η σπαστική
παραπληγία 3A (SPG3A), τo σύνδρομο MARFAN, η
αυτοσωματική υπολειπόμενη πολυκυστική
νόσος των νεφρών (ARPKD), η νευροϊνωμάτωση
τύπου 1 (NF1) και η μυοτονική δυστροφία
τύπου 1 (DM1). Όλα τα παραπάνω νοσήματα
εμφανίζουν βαρύτατη κλινική εικόνα, η
ΚΙ όμως σχετίζεται επί πλέον με την
ανδρική υπογονιμότητα. Στον Ελληνικό
πληθυσμό άνδρες με συγγενή έλλειψη
σπερματικού πόρου είναι κατά 70% τουλάχιστο
φορείς της νόσου, ενώ άνδρες με αποφρακτική
αζωοσπερμία κατά 30%.
Τα μεσογειακά σύνδρομα και η ΚΙ είναι τα δύο πιο συχνά νοσήματα στον Ελληνικό πληθυσμό. 10% του πληθυσμού είναι φορείς β μεσογειακής αναιμίας και άλλων αιμοσφαιρινοπαθειών, όπως δρεπανοκυτταρική αναιμία, και 5% του πληθυσμού είναι φορείς ΚΙ. Τόσο η ΚΙ όσο και τα μεσογειακά σύνδρομα παρουσιάζουν μεγάλη φαινοτυπική και κλινική ετερογένεια στη χώρα μας. Περισσότερες από 80 σημειακές μεταλλάξεις έχουν εντοπιστεί στο CFTR γονίδιο που ευθύνεται για την ΚΙ και περισσότερες από 25 στο β γονίδιο της αιμοσφαιρίνης. Με βάση τα δεδομένα ότι το 85% των μεταλλάξεων στο CFTR γονίδιο εντοπίζονται σε 7 από τα 27 εξόνια του γονιδίου και το 97% στο β γονίδιο αιμοσφαιρίνης εντοπίζονται στο πρώτο μισό του γονιδίου, σχεδιάσαμε και βελτιστοποιήσαμε δύο ευέλικτα και εύκολα προσαρμοζόμενα, ανά περιστατικό, πρωτόκολλα.
Μεσογειακά σύνδρομα
Για
τα μεσογειακά σύνδρομα η μεθοδολογία
που εφαρμόζουμε βασίζεται στον
πολλαπλασιασμό με PCR του πρώτου μισού
του β γονιδίου της αιμοσφαιρίνης, στο
οποίο εντοπίζονται οι περισσότερες από
τις, υπεύθυνες για τα μεσογειακά σύνδρομα
μεταλλάξεις. Ταυτόχρονα πολλαπλασιάζονται
(multiplex PCR) τρεις πολυμορφικές μικροδορυφορικές
αλληλουχίες που βρίσκονται σε σύνδεση
με το β γονίδιο. Η ανίχνευση των μεταλλάξεων
γίνεται στη συνέχεια με εμφωλιαζόμενο
PCR (nested PCR) πραγματικού χρόνου (real-time PCR,
σύστημα LightcyclerTM της Roche), ενώ οι πολυμορφικές
αλληλουχίες αναλύονται φθορισμομετρικά
με ηλεκτροφορητικό διαχωρισμό των
μεγεθών (fragment analysis). Με εκτίμηση των
μεγεθών μεταξύ γονεϊκών και εμβρυϊκών
αλληλομόρφων (linkage analysis) γίνεται έμμεση
διάγνωση, ενώ ταυτόχρονα ελέγχεται και
η πιθανότητα επιμόλυνσης από ξένο DNA σε
κάθε μεμονωμένο κύτταρο. Η μέθοδος
εξασφαλίζει τη διάγνωση του 95% των
μεταλλάξεων στον Ελληνικό πληθυσμό
εντός 6 έως 7 ωρών από την παραλαβή των
κυττάρων βιοψίας, και μπορεί να εφαρμοστεί
και σε άλλους πληθυσμούς.
Κυστική Ίνωση
Για
την ΚΙ το πρωτόκολλο που έχει σχεδιαστεί
επιτρέπει με βάση το γονότυπο των
υποψήφιων γονέων, ταυτόχρονα, τον
πολλαπλασιασμό σε μία PCR (multiplex PCR)
οποιουδήποτε συνδυασμού των 7 εξονίων
του CFTR γονιδίου (4, 10, 11, 13, 14b, 17b, 21) μαζί
με δύο πολυμορφικές ενδογονιδιακές
μικροδορυφορικές αλληλουχίες στα εσόνια
1 και 8. Στη συνέχεια τα εξόνια αυτά
πολλαπλασιάζονται ξεχωριστά με
εμφωλιαζόμενο PCR (nested PCR) και αναλύονται
με ηλεκτροφόρηση σε πήκτωμα ακρυλαμίδης
με αυξανόμενη συγκέντρωση αποδιατακτικών
ουσιών (denaturing gradient gel electrophoresis, DGGE). Οι
μικροδορυφορικές αλληλουχίες αναλύονται
φθορισμομετρικά με ηλεκτροφορητικό
διαχωρισμό. Το πρωτόκολλο αυτό εξασφαλίζει
τη γενετική διάγνωση περισσότερων από
το 75% των συνδυασμών των γονοτύπων που
συναντώνται στον ελληνικό πληθυσμό.
Εφ’ όσον οι μικροδορυφορικές αλληλουχίες
είναι πληροφοριακές, μπορεί να γίνει
και έμμεση διάγνωση, ενώ ελέγχεται και
η πιθανότητα επιμόλυνσης από ξένο DNA.
Άλλα νοσήματα
Για
την ΠΓΔ φυλοσύνδετων ή φυλοεξαρτώμενων
νοσημάτων σχεδιάστηκε και προτυποποιήθηκε
ένα πολλαπλό PCR (multiplex PCR), στο οποίο
πολλαπλασιάζονται 9 διαφορετικοί
γενετικοί τόποι χαρακτηριστικοί για
τα φυλετικά χρωμοσώματα. Η μέθοδος
επιτρέπει τον προσδιορισμό του φύλου
σε ένα κύτταρο. Παράλληλα, ανάλογα με
το νόσημα που ενδιαφέρει κάθε φορά,
ενσωματώνεται στον πολλαπλασιασμό και
το τμήμα του γονιδίου που σχετίζεται
με το συγκεκριμένο νόσημα, όπως του
γονιδίου της δυστροφίνης ή του γονιδίου
STAR (στην μυϊκή δυστροφία Duchenne ή στην
λιποειδή υπερπλασία των επινεφριδίων
αντίστοιχα).
Το πρωτόκολλο για ΠΓΔ της νωτιαίας μυϊκής ατροφίας (SMA) βασίζεται σε πολλαπλασιασμό του φυσιολογικού γονιδίου SMN με τη μέθοδο allele specific PCR, γνωστή ως ARMS. Παράλληλα πολλαπλασιάζονται δύο μικροδορυφορικές πολυμορφικές αλληλουχίες δεξιά και αριστερά του γονιδίου, ώστε να γίνεται ταυτόχρονα έμμεση επιβεβαίωση της ύπαρξης του φυσιολογικού γονιδίου αλλά και έλεγχος επιμόλυνσης.
Στην περίπτωση όλων των υπολοίπων μονογονιδιακών νοσημάτων (γλυκογονίαση, συγγενής αμαύρωση Leber, σπαστική παραπληγία, σύνδρομο Marfan, αυτοσωματική υπολειπόμενη πολυκυστική νόσος των νεφρών και νευροϊνωμάτωση τύπου 1), με βάση τις μεταλλάξεις των υποψήφιων γονέων που ζήτησαν ΠΓΔ, πολλαπλασιάζεται το τμήμα του γονιδίου στο οποίο εντοπίζονται οι γονεϊκές μεταλλάξεις, παράλληλα με δύο τουλάχιστον συνδεδεμένες πολυμορφικές μικρoδορυφορικές αλληλουχίες.
Στην περίπτωση της μυοτονικής δυστροφίας τύπου 1 το πρωτόκολλο που εφαρμόζεται αφορά στον πολλαπλασιασμό του φυσιολογικού αλληλόμορφου από τον κάθε γονέα, καθώς το παθολογικό αλληλόμορφο είναι πολύ μεγάλο ώστε να μπορεί να ανιχνευτεί με απλό PCR. Η χρήση δύο μικροδορυφορικών αλληλουχιών σε σύνδεση με το γονίδιο DMPK, επιτρέπει παράλληλα την έμμεση επιβεβαίωση της διάγνωσης, όπως σε προηγούμενα πρωτόκολλα.
Στο διάστημα των 13 τελευταίων ετών παρατηρείται στο Εργαστήριο Ιατρικής Γενετικής ετησίως μια σταθερή αύξηση του αριθμού των ζευγαριών που αποφασίζουν να μπουν στην διαδικασία της ΠΓΔ (κύκλος Εξωσωματικής γονιμοποίησης – IVF - σε συνδυασμό με ΠΓΔ), ξεπερνώντας τους 60 κύκλους ετησίως. Στο διάστημα αυτό ζήτησαν να ενημερωθούν για τη διαδικασία της ΠΓΔ 371 ζευγάρια και από αυτά τα 287 ξεκίνησαν έναν τουλάχιστο κύκλο, συνολικά 494 κύκλοι. Στους 426/494 κύκλους πραγματοποιήθηκε τελικά ΠΓΔ αφού το 25-30% των κύκλων διακόπτονται λόγω μειωμένης ορμονικής ανταπόκρισης, με μικρό αριθμό ή κακής ποιότητας ωάρια. Η γενετική διάγνωση έγινε είτε σε βλαστομερίδια, είτε σε κύτταρα από την εξωτερική στοιβάδα βλαστοκύστης. Η γενετική διάγνωση ήταν εφικτή σε περισσότερα από το 93% των εμβρύων που υποβλήθηκαν σε βιοψία. Μέχρι σήμερα έχουν γεννηθεί 156 φυσιολογικά νεογνά.
Προβληματισμοί
Κατά
την κλινική εφαρμογή ΠΓΔ αναδεικνύονται
κάποια ηθικά διλήμματα και προβληματισμοί,
όπως στις ακόλουθες περιπτώσεις:
α)
ΠΓΔ με σκοπό τη γέννηση συμβατού αδελφού
δότη (HLA typing). Στόχος είναι η μεταμόσχευση
σε προϋπάρχον παιδί στην οικογένεια
που πάσχει από ανίατη ασθένεια. Τέτοιες
ασθένειες μπορεί να είναι διάφορες
λευχαιμίες, η αναιμία Fanconi, η β Μεσογειακή
Αναιμία κ.α. Είναι γνωστό ότι η μεταμόσχευση
μυελού των οστών είναι περισσότερο
αποτελεσματική και ασφαλής όταν ο δότης
έχει συγγενική σχέση με τον πάσχοντα.
Όταν δεν υπάρχει αδελφός δότης οι γονείς
συχνά καταφεύγουν στην ΠΓΔ. Στο σημείο
αυτό όμως προβάλλουν κάποια ηθικά
διλήμματα όπως: πόσο ηθικό είναι να
εμποδίσεις ένα φυσιολογικό έμβρυο να
εξελιχθεί σε ανθρώπινο ον επειδή δεν
πληροί το κριτήριο της ιστοσυμβατότητας;
ή πόσο επώδυνο ψυχολογικά είναι για το
ιστοσυμβατό φυσιολογικό αδερφάκι να
γνωρίζει πως ήρθε στον κόσμο, κατά
παραγγελία, για να σωθεί κάποιος άλλος
και όχι γιατί ο ίδιος ήταν επιθυμητός
από τους γονείς του; Υπάρχει όμως και ο
αντίλογος ότι ο συμβατός αδελφός δότης
όχι μόνο είναι πολύ επιθυμητός από την
οικογένεια αλλά και ότι επιπροσθέτως,
η σημαντική του προσφορά, σώζοντας το
άρρωστο αδερφάκι του, τον κάνει ακόμα
περισσότερο ξεχωριστό στα μάτια των
γονιών του και κατά συνέπεια αποδεκτό
και αγαπητό από ολόκληρη την οικογένεια.
Επιπλέον ακόμη και αν η μεταμόσχευση
αποτύχει και το πρώτο παιδί χαθεί, οι
γονείς θα έχουν το δεύτερο παιδί για να
αγαπούν. Σε καμιά περίπτωση δεν περιμένει
κανείς από γονείς που έχουν την ευαισθησία
να σώσουν το άρρωστο παιδί τους μπαίνοντας
στην επίπονη διαδικασία της ΠΓΔ, να
αγνοήσουν τις ανάγκες ενός δεύτερου
παιδιού στην οικογένεια ή να μην το
αγαπήσουν και αυτό. Ο Οργανισμός
Εμβρυολογίας & Ανθρώπινης Γονιμοποίησης
στην Αγγλία (ΗFEA -Human Fertilisation and Embryology
Authority, www.hfea.gov.uk) αποδέχεται την ΠΓΔ για
HLA ιστοσυμβατότητα μόνο στην περίπτωση
των νοσημάτων που και το δεύτερο παιδί
έχει κίνδυνο να νοσήσει (π.χ. στην αναιμία
Fanconi), όχι όμως για νοσήματα που δεν
υπάρχει κληρονομικότητα (π.χ. λευχαιμία
ή λέμφωμα). Η θέση αυτή όμως δεν υιοθετείται
από άλλες χώρες όπου εφαρμόζεται ΠΓΔ
ακόμη και με μόνη ένδειξη την HLA
ιστοσυμβατότητα. Πρέπει όμως να τονιστεί
ότι, στην απόφαση για την επιλογή της
ΠΓΔ ως λύση για την εύρεση συμβατού
δότη, σημαντικό είναι να συνεκτιμηθεί
από την οικογένεια και η πιθανότητα που
υπάρχει ώστε να βρεθεί συμβατός αδελφός
δότης, αφού η συνδυασμένη διάγνωση
(νόσημα και συμβατότητα) μειώνει τα
αναμενόμενα ποσοστά των κατάλληλων
εμβρύων για εμβρυομεταφορά. Από πρακτικής
απόψεως οι αναμενόμενες πιθανότητες
είναι 25% για απλή ιστοσυμβατότητα, 18.8%
για ιστοσυμβατότητα σε συνδυασμό με
υπολειπόμενο μονογονιδιακό νόσημα και
μόνο 12.5% για ιστοσυμβατότητα σε συνδυασμό
με φυλοσύνδετο νόσημα. Και τα δυο παραπάνω
πρωτόκολλα παρέχουν τη δυνατότητα
εντοπισμού







Σχόλια